���л�ѧ����ʽ��ƽ����
���л�ѧ����ʽ���ڻ�ѧѧϰ��˵�dz���Ҫ���������ʱ���������ʽû����ƽ����ô���ǵ����û����������������С�������ĸ��л�ѧ����ʽ��ƽ���������ο���
һ����С��������
���岽�裺
1.�ҳ���Ӧʽ��������ԭ��������ijһֻ����һ�ε�Ԫ�أ�������ǵ���С��������
2��������С�������ֱ������������ԭ����ԭ����������֮��ֵ���ͷֱ����������ڻ�ѧʽ��ϵ����
3��������ȷ�������ʻ�ѧʽ��ϵ�����Ƶ������������ѧʽ��ϵ����ֱ��������ʽ��ƽΪֹ��4����֤��Ӧʽ����ƽ�Ƿ���ȷ��
[��1]����ƽ������fe3o4�����۹�ȼ�ķ�Ӧ����fe3o4ʮal����feʮal2o3
(1)�÷�Ӧ��ԭ�����϶���������ֻ����һ�Σ�
�������������ԭ��������С��������4��3��12��
��2�����������غ㶨�ɣ�Ҫʹ��Ӧʽ�������ߵ���ԭ������ȣ�fe3o4��ϵ������Ϊ3(12��4)��al2o3��ϵ������Ϊ4(12/3)����
3fe3o4ʮa1����feʮ4al2o3
��3������fe��alԭ�ӡ�������õ�fe3o4��4al2o3��֪��fe��al��ϵ���ֱ�Ϊ9��8ʱ���������ߵ�fe��al��ԭ��������ȣ����У�
3fe3o4+8al����9fe+4al2o3
(4)�����飬�������Ļ�ѧ����ʽΪ��
3fe3o4+8al======9fe+4al2o3
1��al+o2����al2o32��al+h2so4����al2��so4��3+h2
3��fe+o2����fe3o44��al+mno2����mn+al2o3
5��n2+h2����nh3
�����۲취
���岽�裺��1���ӻ�ѧʽ�ϸ��ӵ�һ�������������йط�Ӧ�ﻯѧʽ�Ļ�ѧ����������һ������Ļ�ѧ����������2��������õĻ�ѧʽ�Ļ�ѧ�����������ҳ�������ѧʽ����й������������������ƽ��
���磺fe2o3+co����fe+co2
�۲죺
���ԣ�1��fe2o3Ӧ��3����o���ֱ��3��co��ʹ��ת��Ϊ3��co2����fe2o3+3co����fe+3co2�ٹ۲���ʽ�������2��fe��fe2o3���������ұ�fe��ϵ��ӦΪ2����
fe2o3+3co����2fe+3co2
�����͵õ���ƽ�Ļ�ѧ����ʽ�ˣ�ע�⽫�������߱�ɡ�=���š���fe2o3+3co==2fe+3co2
1��h2o+fe��fe3o4+h22��c+fe2o3����fe+co2
3��co+fe3o4����fe+co24��c+fe3o4����fe+co2
����������ż����
ѡ��Ӧǰ��ѧʽ��ԭ�Ӹ���Ϊһ��һż��Ԫ������ƽ��㣬���������ż����Ȼ������ƽ����Ԫ��ԭ�ӵķ�����Ϊ������ż������
���磺����(ch4)ȼ�շ���ʽ����ƽ���Ϳ��Բ���������ż������ch4+o2�D�Dh2o+co2����Ӧǰo2����ԭ��Ϊż��������Ӧ��h2o����ԭ�Ӹ���Ϊ�������Ƚ�h2oǰ����2����ԭ�Ӹ�����������Ϊż����ch4+o2�D�D2h2o+co2������ƽ����Ԫ�ص�ԭ�ӣ�ch4+2o2==2h2o+co2��
�ġ���һ��
�ҵ���ѧ����ʽ�йؼ��Ļ�ѧʽ�����仯ѧʽǰ������Ϊ1��Ȼ����ݹؼ���ѧʽȥ��ƽ������ѧʽǰ�Ļ�ѧ�������������ּ�����Ϊ�������ٽ���������ͬ����ͬһ������������Ϊ�����������ȶ��ؼ���ѧʽ������Ϊ1����ƽ��������Ϊ��һ����
���磺�״�(ch3oh)ȼ�ջ�ѧ����ʽ��ƽ�ɲ��ô˷���ch3oh+o2�D�Dh2o+co2����Ȼ��������h2o��co2�Ķ��ٵĹؼ��Ǽ״�����ɣ�������������Ϊ1�������ɵ���ȼ�պ�����h2o��co2�ķ��Ӹ�����ch3oh+o2�D�D2h2o+co2��Ȼ����ƽ��ԭ�ӣ�ch3oh+3/2o2===2h2o+co2������������ͬ����2����Ϊ������2ch3oh+3o2==4h2o+2co2��
�塢���ϼ�������
�껯�ϼ�:��ѧ�ߵĻ�������ʽ������Ԫ�صĻ��ϼ۶��������Ȼ���ҵ����ϼ����ߺͽ��͵�Ԫ�أ��Ƚ���Ϥ֮��Ϳ���ֻ�귢���仯��Ԫ�صĻ��ϼۣ�����ͼ�е���ĿΪ�����������Ԫ�صĻ��ϼۡ�
�����������:�ҵ����ߺͽ��͵�Ԫ��֮����Ԫ���ǴӼ������ߵ����ۣ����ǴӼ��۽��͵����ۡ���Ŀ�У�̼Ԫ�ش�0�����ߵ�+4�ۣ�������4�ۣ���Ԫ�ش�+5�۽��͵�+4�ۣ�������1��
ȷ�����ʵ�ϵ��:��ȷ����������ݵ�ʧ�����غ㣬�ҵ����ߵĻ��ϼۺͽ��͵Ļ��ϼ۵���С����������Ŀ�У�������4�ۣ�������1�ۣ���ô�ҵ�4��1����С��������4����ô4X1��1X4����ô���C��ϵ��Ϊ1�����HNO3��ϵ��Ϊ4
Tags����ѧʽ ����ʽ ������ ��� fe ��ԭ�� fe3 ��Ӧʽ 2o ���л�ѧ
�������
-
2025-10-14

���¸��л�ѧ����ʽ��ȫ324����������궼�õ��ϣ�
��ȫ���ܣ��Ͽ��ղ�
-
2025-09-08
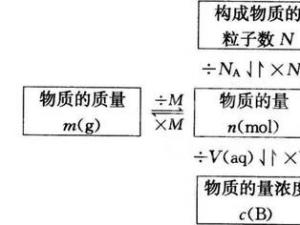
���л�ѧ������һ�������ȫ
һ����Ϥ��ѧʵ���������Σ�ջ�ѧƷ��־����ƾ������͡�����ȼҺ�壻ŨH2SO4��NaOH����������ʴƷ���������ķ�����ᴿ��1������ķ������ٹ��ˣ�����(����)��Һ��ķ��롣������������(����)��Һ����롣�����е㲻ͬ��Һ������ķ��롣�ܷ�Һ���������ܵ�Һ���������ȡ������..
-
2025-09-02

���л�ѧ���ã�Ԫ�����ڱ�����ھ��̸���
��һ�����ڣ��⺤�����\�ֺ����������������ɡ��ڶ����ڣ������̼�������ʣ���Ƥ��̿�������̣���ǰһ�����ú���Ƥ��ľ̿����һ����˵���Ǵӵ������Ķ������̡��������ڣ���þ����������벣������ù飬����·ѽ����һ���˴������������л�������·���кܶ������������ڣ��ظ����ѷ�����������ͭп..
����ϲ��
-
2025-05-19
ƭ���緹
1���߿�������ѧ������ˬ��С��˯�����������أ�������ң�ͬѧ���ѣ����а�Сʱ�����ˣ��������������ʪ��û��װ��...2����һ�������¿η����оŸ�δ�ӵ绰���������ͻع�ȥ�ˣ��ǿ��Ա��ģ����Ա�ʣ����Ͽζ������ֻ����𣿶�������˯���ˡ���3�������ϿΣ�û����һ�����ǣ��˸羭������..
-
2023-10-07
�����ֳ�,����Цſ��
1��С���һ��Ů���ӵ����ֱ���͵�ˣ�һ���������������ĸ������Ӹ�͵��������֣���MD��Сʱ��û�̳�����������̵����ֻؼ�������ȫ��С��Цſ�ˡ�2�������ڳ��տ�ʱ������һ�����³��ų������ˡ���Ȼ����Ů���ܹ���������һ�£�Ȼ�����е��������ڵ��ܹ�����Ҳ������һ�¡��������ո�ȥ..
-
2023-08-11
˾�������Ѻͷ�������Ĭ
1�����٣�������͵������ʱ���ѵ���û������������Ÿ���ô�죿��С͵��������ˣ�������̵�����û��Ůʿ�·���2��һ�˱�Ź��Pol.ice�ϵ��ֳ�������Pol.ice�ʱ�Ź����ˣ�����������������˵���ò�𣿡�����ί���ػش𣺡���Ȼ�ܣ��Ҿ�����Ϊ�����������Ӷ�����ģ�3��������ðɣ���С����..
-
2021-08-02
ͬѧ,����������!
1���ң��ĸ�˲����������Լ���ĺ��ͬѧ��ظ���������������¥����û�н赽ŵ�����ֻ��ij������2�������潨�˸�Ⱥ��ͬѧ��ʦ�������档ͻȻ�и�ͬѧ�����Ű�����(Ů)��Ƭ��������һ�飬���˸���ߣ��Ȼ��ֲ�����������ˣ���������Ⱥ�ˡ�����3������������̸��˵�����ҹ��ĵ�������ϵͳ��һ��..
-
2021-06-03
(�ֲ�)��������亹,�������Ů�����ԣ�
��1����������ѧ��������һ��ʵ�顣��������һ���ˣ��������ߣ�������˵���Լ���ǰ��������ͽ�����ʱ��ģ����2���ҵ�һ�����Ѿ���ô������ȥ������һ���ڼ����ĵ����Լ��ҵ绰��ͨ�Լ��ҵ绰���ܶ�κ����ڲ�ͨ�ˣ�������һ���ն���������������һ�������Ȳ��һ���ˮ�ε��������ڶ�����ʧ���ˣ���..
- �߶���ѧ�κ���ϰ�⣺���ĺ�����������𰸽�����
- ���л�ѧ֪ʶ���⡪�������ܽ�ƽ���е�ͬ����ЧӦVS��ЧӦ
- ʲô�����Ӽ�_ʲô�ǹ��ۼ�_���Ӽ��빲�ۼ��ıȽ�
- ʵ�����Ʊ���������ʱ�����÷�����ȷ����
- �ҹ��Ŵ����û��տ�ȸʯ�ͽ�̿�����ķ�����ͭ����ȸʯ����..
- ʲô�ǻ�ѧ�������Ӽ������������_��ѧ�������Ӽ�����������..
- ��һ��ѧ����ĩ��ѧԤ���������⣬�ɴ�ӡ��ѧ����������..
- ��ѧ��һ�ż����ʵ��Ŀ�ѧ